- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
2025年4月173項進口第一類醫療器械產品備案事項獲批 來自國家藥監局2025年5月16日披露的數據,2025年4月173項進口第一類醫療器械產品備案事項獲批,其中,新增進口第一類醫療器械產品備案54項;進口第一類醫療器械產品備案變更112項;進口第一類醫療器械產品備案無效7項。 時間:2025-5-16 22:33:55 瀏覽量:575

-
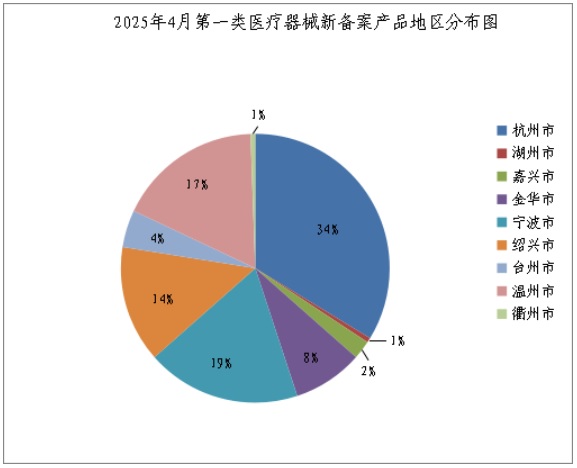
31個溫州市第一類醫療器械產品備案獲批(2025年4月) 來個浙江省藥品監督管理局近日披露的數據,2025年4月,浙江省內各市市場監督管理局共新備案第一類醫療器械產品178個,其中有源類6個,無源類73個,體外診斷試劑99個。其中,杭州市第一類醫療器械產品備案60個,寧波市第一類醫療器械產品備案33個,溫州市第一類醫療器械產品備案31個,紹興市第一類醫療器械產品備案25個,金華市第一類醫療器械產品備案15個。 時間:2025-5-15 22:33:48 瀏覽量:556
-
醫療器械注冊答疑之醫療器械末道清洗要求 對于部分醫療器械注冊產品有末道清洗工序,有關醫療器械末道清洗的法規要求如下:對于直接或間接接觸心血管系統、淋巴系統或腦脊髓液或藥液的無菌醫療器械,若用于末道清洗應當使用符合《中國藥典》要求的注射用水或用超濾等其他方法產生的同等要求的注射用水。 時間:2025-5-15 0:04:00 瀏覽量:979

-
國家藥監局2025年4月批準進口醫療器械注冊產品41個 來自國家藥監局2025年5月13日披露的數據,2025年4月,國家藥監局共批準注冊醫療器械產品266個。其中,境內第三類醫療器械產品225個,進口第三類醫療器械產品30個,進口第二類醫療器械產品11個。 時間:2025-5-13 20:52:40 瀏覽量:896

-
《免于進行臨床評價醫療器械目錄(2025年)》今日發布,即日實施! 2025年5月13日,為做好醫療器械注冊管理工作,根據《醫療器械注冊與備案管理辦法》(國家市場監督管理總局令第47號),國家藥監局組織修訂了《免于進行臨床評價醫療器械目錄(2023年)》(國家藥監局通告2023年第33號),形成《免于進行臨床評價醫療器械目錄(2025年)》,現予公布,并自公布之日起施行。 時間:2025-5-13 20:40:56 瀏覽量:870
-
醫療器械注冊質量管理體系之關鍵工序每年需要驗證嗎? 對于醫療器械注冊質量管理體系或是ISO13485認證來說,關鍵工序和特殊工序都是過程管控的重點,今天有客戶朋友問到,關鍵工序每年需要驗證嗎?考慮到問題的典型性,因此,寫個文章,說說這個事。 時間:2025-5-12 22:20:08 瀏覽量:932

-
電子血壓計注冊申報時,如何提交臨床準確度驗證報告? 盡管電子血壓計在免于開展醫療器械臨床試驗目錄之內,但是由于電子血壓計的測量特性,在電子血壓計注冊申報時,仍然需要提交臨床準確度驗證報告。本文為大家說說電子血壓計產品在申報首次注冊/變更注冊過程中執行YY 9706.230時,如何提交電子血壓計臨床準確度驗證報告,一起看正文。 時間:2025-5-11 20:59:50 瀏覽量:1042

-
歸屬于第二類醫療器械器械注冊管理的磁療產品命名需注意什么? 對于醫療器械注冊產品來說,產品命名適用醫療器械命名規則,并有具體的要求和禁止用語,本文為大家介紹歸屬于第二類醫療器械器械注冊管理的磁療產品命名注意事項,一起看正文。 時間:2025-5-11 20:51:42 瀏覽量:715

-
移動醫療器械注冊審查指導原則(2025年修訂版) 為進一步規范移動醫療器械的管理,國家藥監局器審中心組織制定了《移動醫療器械注冊審查指導原則(2025年修訂版)》,并于2025年5月7日發布,一起來看具體內容。 時間:2025-5-8 21:20:13 瀏覽量:1274

-
2025年度醫療器械注冊審查指導原則編制計劃111項 2025年5月7日,國家藥監局發布《關于發布2025年度醫療器械注冊審查指導原則編制計劃的通告(2025年第10號)》,包括第三類醫療器械注冊審查指導原則制修訂計劃、第二類醫療器械注冊審查指導原則制修訂計劃共計111項。相關醫療器械注冊企業可以積極參與醫療器械注冊審查指導原則的制修訂工作,關注法規動向。 時間:2025-5-8 21:09:04 瀏覽量:988

-
第二類醫療器械延續注冊之既往溝通記錄相關問題 對于第二類醫療器械延續注冊事項來說,需要書面說明申報前聯系情況和與監管機構的既往溝通記錄,本文跟大家說說既往溝通記錄常見發補項,一起看正文。 時間:2025-5-7 22:15:53 瀏覽量:627

-
第二類醫療器械延續注冊之申請表常見問題 對于第二類醫療器械注冊事項來說,醫療器械延續注冊算是相對簡單的事項,但是由于醫療器械注冊本身涉及諸多細節和文字表述,延續注冊也是出現各種各樣的問題,本文為大家說說醫療器械延續注冊申請表常見問題,一起看正文。 時間:2025-5-7 22:05:57 瀏覽量:821

-
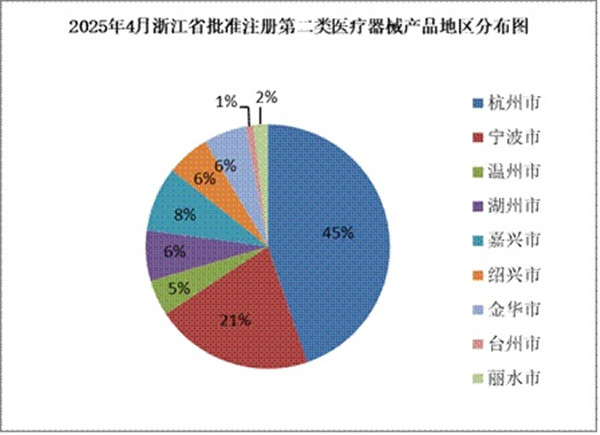
2025年4月浙江省共批準105個第二類醫療器械注冊產品 來自浙江省藥品監督管理局披露的消息,2025年4月,浙江省共批準第二類醫療器械注冊產品105個,按照醫療器械注冊申請人所在轄區分析,杭州市第二類醫療器械注冊產品47個,寧波市第二類醫療器械注冊產品22個,溫州市第二類醫療器械注冊產品5個,湖州市第二類醫療器械注冊產品7個,嘉興市第二類醫療器械注冊產品9個,紹興市第二類醫療器械注冊產品6個,金華市第二類醫療器械注冊產品6個,臺州市1個,麗水市2個。 時間:2025-5-6 0:00:00 瀏覽量:1502
-
江蘇某醫療器械公司使用虛假資料申請醫療器械許可被罰近3600萬元 特別典型的強監管、重處罰的典型醫療器械違法案例,江蘇立峰生物科技有限公司使用虛假資料申請二類醫療器械許可被罰3593.52萬元,處以違法所得20倍罰款金額,并處限制從業處罰。這個案例給所有醫療器械注冊人都是警示,值得大家深思! 時間:2025-5-6 22:26:16 瀏覽量:728

-
《中醫脈診類產品技術審評規范》(2016版)是否已經作廢? 由于地方標準和國家藥監局標準制定單位不一致,有時候會有不同標準存在差異或者沖突的地方。今天,正好有客戶問到我《中醫脈診類產品技術審評規范》(2016版)是否已經作廢這個問題,考慮到中醫脈診設備是近年熱門醫療器械注冊產品之一,因此,寫個文章說說這個事。 時間:2025-5-5 23:22:15 瀏覽量:639

-
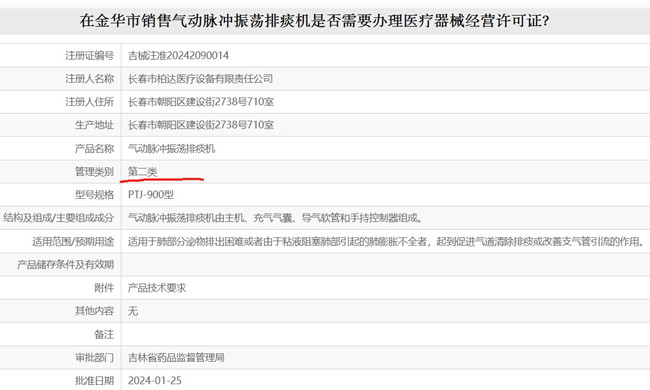
在金華市銷售氣動脈沖振蕩排痰機是否需要辦理醫療器械經營許可證? 適用于肺部分泌物排出困難或者由于粘液阻塞肺部引起的肺膨脹不全者,起到促進氣道清除排痰或改善支氣管引流的作用的排痰機,在臨床上廣泛應用。今天正好有金華市朋友電話問到我有關銷售氣動脈沖振蕩排痰機是否需要辦理醫療器械經營許可證這個話題,寫個文章一并說明。 時間:2025-5-4 23:31:59 瀏覽量:702
-
體外診斷試劑降類產品在延續注冊申請中規范產品預期用途等內容 由于監管技術的發展,醫療器械注冊產品在臨床應用中的良好表現,產品技術發展、產品風險變化等因素,醫療器械產品降類,體外診斷試劑降類是行業常見情況。本文為大家說說體外診斷試劑降類產品在延續注冊申請中規范產品預期用途常見問題。 時間:2025-5-3 0:00:00 瀏覽量:645

-
有源醫療器械增加規格型號,在變更注冊時是否一定要醫療器械注冊檢驗報告? 對于有源醫療器械注冊產品,如果在原有注冊單元的基礎上,醫療器械注冊人希望新增規格型號,在申請醫療器械變更注冊(增加規格型號注冊)時,是否一定要提交醫療器械注冊檢驗報告?考慮到問題的典型性,因此,寫個文章說說這個事。 時間:2025-5-3 22:22:14 瀏覽量:742

-
牙科樹脂類充填材料產品注冊審查指導原則(2025年修訂版) 牙科樹脂類充填材料產品注冊審查指導原則(2025年修訂版),旨在指導注冊申請人對牙科樹脂類充填材料產品注冊申報資料的準備及撰寫,同時也為技術審評部門對注冊申報資料的審評提供技術參考。本指導原則是對牙科樹脂類充填材料產品注冊申報資料的一般要求,注冊申請人需依據產品的具體特性確定其中內容是否適用。若不適用,需具體闡述理由及相應的科學依據,并依據產品的具體特性對注冊申報資料的內容進行充實和細化。 時間:2025-5-2 20:57:14 瀏覽量:829

-
醫療器械軟件注冊之認識系統軟件、應用軟件、中間件、支持軟件 對于醫療器械軟件注冊申請人來說,要理解和掌握許多有別于傳統醫療器械的名詞和術語,比如系統軟件、應用軟件、中間件、支持軟件等等,理解并厘清這些術語,有助于我們規劃軟件管理邊界,并適度開展醫療器械軟件產品的醫療器械質量管理體系建設,一起看正文。 時間:2025-5-2 20:44:44 瀏覽量:646

